ИЗБЫТОЧНАЯ ЗАБОЛЕВАЕМОСТЬ РАКОМ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ПРИ ВНЕШНЕМ ВОЗДЕЙСТВИИ ИОНИЗИРУЮЩЕЙ РАДИАЦИИ НА ПЕРСОНАЛ
ИЗБЫТОЧНАЯ ЗАБОЛЕВАЕМОСТЬ РАКОМ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ПРИ ВНЕШНЕМ ВОЗДЕЙСТВИИ ИОНИЗИРУЮЩЕЙ РАДИАЦИИ НА ПЕРСОНАЛ
Аннотация
Проведено повторное статистико-эпидемиологическое исследование радиогенного риска заболевания раком предстательной железы в когорте ПО «Маяк», включавшей 19 395 мужчин. Его цель состояла в выявлении фактической наблюдаемой связи между воздействием ионизирующей радиации и групповым риском развития заболевания в условиях хронического облучения на рабочих местах. Выявлена сравнительно высокая и статистически значимая доля радиационно-обусловленных событий развития заболевания в когорте – около 42% (ДИ: 28 – 53%) из 298 случаев. Период наблюдения – от начала работы предприятия до конца 2013 года. Использованы преимущественно оценки доз внешнего гамма-облучения стенки мочевого пузыря, которые имеются в дозиметрической системе MWDS-2013. По показателю Нельсона-Аалена на возрастном интервале от 25 до 75 лет коэффициент дозового тренда избыточного кумулятивного риска составил примерно от 20% до 40% на 1 Зв эквивалентной дозы в зависимости от её кумулятивной величины, близкой к средним показателям по когорте. Оценки выполнены как непараметрическими методами, так и с использованием алгоритма AMFIT, с учётом исправления его недокументированных особенностей и коррекции параметрических моделей.
Особое внимание в работе уделяется анализу причин, по которым в аналогичных исследованиях на других когортах не всегда удавалось найти статистически значимую связь прироста заболеваемости с облучением на рабочих местах. Установлено, что, главным образом, это было вызвано либо отсутствием подходящего инструмента выполнения статистических оценок, либо некорректным использованием статистических моделей при описании категорий «эффект» и «радиационный эффект».
1. Введение
Рак предстательной железы (РПЖ; С61 по коду МКБ-10) – одно из наиболее распространённых злокачественных новообразований у мужчин. В структуре заболеваемости раком среди мужчин России РПЖ занимает второе место после рака легкого, бронхов и трахеи (С33, С34) . На некоторых территориях, например в штате Невада (США), известном наземными и воздушными испытаниями ядерного оружия, заболеваемость РПЖ может выходить на первое место, несмотря на то, что основная часть населения на территории штата имеет совсем небольшое избыточное (по сравнению с естественным фоном) радиационное облучение . В таких условиях вполне закономерным является предположение о возможной существенной связи между повышенной заболеваемостью и радиацией, однако актуальным является установление её силы. Такая задача осложняется по двум основным причинам. Во-первых, установлено несколько факторов роста показателей заболеваемости РПЖ, наряду с возможным действием радиации. Во-вторых, не найдено специфических гистологических признаков, позволяющих отличить радиогенный РПЖ от спонтанного по результатам медико-биологического обследования. Единственный доступный инструмент – статистико-эпидемиологическое исследование больших неоднородных когортных или популяционных выборок индивидуумов в широком диапазоне возрастов наблюдения с целью определения дозового тренда. Однако такие исследования требуют существенных трудозатрат, финансовых средств, времени наблюдения, а также применения специфического статистического инструментария. Поэтому попытки установления связи между РПЖ и радиацией очень редки и не всегда убедительны. Более того, результат может быть зависящим от выбора контролируемого статистического показателя, являющегося мерой «эффекта».
Автору известно четыре регистра, с которыми проводилась работа по установлению статистической связи между воздействием ионизирующей радиации и заболеваемостью РПЖ или смертностью. Это – национальный регистр работников радиационных производств Англии (The National Registry for Radiation Workers, NRRW); объединенный регистр ядерных производств США под мониторингом национального института охраны труда (The National Institute for Occupational Safety and Health, NIOSH); когорта лиц, переживших атомные бомбардировки Хиросимы и Нагасаки (Life Span Study, LSS); а также – регистр работников ПО «Маяк». Хронологически первыми , явились попытки исследования связи с дозой гамма-, альфа- и бета-излучения величины отношения стандартизированных (усредненных по возрастному распределению в популяции) показателей смертности (Standardized Mortality Ratio, SMR) в регистре английских работников. Связь обнаружена не была. Возможное объяснение – существенно неравномерная чувствительность показателя смертности в разных возрастных интервалах наблюдения или к разным источникам ионизирующей радиации. На это указывает обнаруженная искомая связь при использовании другого кумулятивного показателя – относительного риска – в методе исследования «случай – контроль» при действии специфического радионуклида (тритий тяжеловодных реакторов и изотопы цезия; табл. 3 в работе ). Исследование годовых показателей интенсивности смертности от РПЖ также не выявило связи с кумулятивной дозой гамма-излучения в когорте LSS . Раздел, посвященный заболеваемости РПЖ в , вообще заканчивается словами: «Из-за небольшого числа случаев ... <(387)> ... было невозможно сделать выводы о дозовом тренде эффекта для этой локализации рака». Ввиду отсутствия убедительных результатов, тема исследования влияния ионизирующей радиации на повышенную смертность от РПЖ или заболеваемость не поднималась в течение 30 лет до тех пор, пока в рамках линейно-беспороговой гипотезы по показателю интенсивности заболеваемости не был выполнен многофакторный анализ дозового тренда для 160 случаев заболевания РПЖ у 16685 мужчин – работников радиационно-опасного предприятия , . Как оказалось, он был статистически значим для всей когорты , а в возрасте 50 лет коэффициент дозового тренда избыточного относительного риска (ИОР) достигал 5,24 на 1 Гр. Парадоксально, но авторы связали столь значительный прирост всего лишь с незначительными 5 избыточными случаями радиогенного РПЖ. Через короткое время многофакторный анализ дозового тренда по показателю интенсивности заболеваемости был выполнен уже для японской когорты LSS , , превышающей когорту ПО «Маяк» примерно пятикратно по числу «случаев» (851 заболевание РПЖ в когорте из 41 544 мужчин), но уступающей ей по средним дозовым уровням. При этом оценен линейный тренд годового показателя риска по кумулятивной дозе с коэффициентом ИОР/Гр = 0,57 (95% ДИ: 0,21-1,00), однако не обнаружено влияния курения, потребления алкоголя, индекса массы тела и возраста на момент облучения на величину риска развития РПЖ. Может сложиться неожиданное впечатление, что связь «доза – риск» характерна только для острого радиационного воздействия, а при хроническом облучении она не является статистически значимой при производственных уровнях доз.
Таким образом, можно констатировать, что проблема оценки связи заболеваемости РПЖ с действием ионизирующей радиации всё ещё достойна более тщательного исследования, так как убедительных выводов о существовании или отсутствии связи РПЖ с облучением не получено. Можно предположить, что некоторая взаимная противоречивость публикаций , , , вызвана тем, что они либо выполнены на недостаточном массиве данных, либо опираются на существенно отличающиеся меры эффекта, либо содержат некие неединичные методологические ошибки, приводящие к разнонаправленной интерпретации результатов. Здесь уместно отметить, что большинство оценок, исключая работы , , , выполнены с помощью пакета статистической обработки данных Epicure с использованием модулей AMFIT и DATAB, а работа опирается на оценки относительного риска или отношения шансов по алгоритму Бреслоу и Дея , реализованному в модуле PECAN, также в составе пакета Epicure.
Нет ответа, объясняется ли взаимная несогласованность ранее проведённых исследований спецификой локализации РПЖ, или это связано с недостатками методики, либо с ошибками в практике применения статистического инструментария. Целью данной публикации является прямая оценка связи РПЖ и радиационного воздействия, а также выявление роли способа статистической интерпретации результатов.
2. Материал и методы
Для оценки связи «доза – риск» может быть предложена следующая двухступенчатая схема исследования. На первом этапе – прямая оценка существования связи с помощью двух непараметрических методов – а) кумулятивного и б) традиционного исследования интенсивности заболеваемости в отдельных условно однородных возрастных подгруппах. На втором этапе – проверка возможности подтверждения полученных выводов с помощью параметрического метода максимального правдоподобия (ММП) для стратифицированной когорты. В последнем случае будет использован алгоритм AMFIT, вместе с его методическими коррекциями. Иными словами, выполним разведочный анализ и анализ воспроизводимости результатов средствами общепризнанного инструмента (как известно, пакет Epicure позиционируется своими создателями как фактический стандарт радиационно-эпидемиологических исследований: «… Epicure is the de-facto standard for modeling radiation health effects …» ).
В качестве источника данных в анализе использован регистр персонала ФГУП ПО «Маяк», содержащий индивидуальные записи об уровнях радиационного воздействия и нерадиационных факторов риска для работников трех заводов основного производства и ряда вспомогательных производств. Общая численность по состоянию на 31.12.2013 составила 19 395 мужчин. Исследуемый эффект – радиогенная заболеваемость РПЖ, то есть ставится задача выявления повышенной интенсивности заболеваемости по отношению к фоновым показателям, присущим мужчинам исследуемой когорты. Наряду с интенсивностью анализировались также и кумулятивные показатели. Рассмотренный регистр мало отличается от своего прототипа, рассмотренного в работе , где анализировалась заболеваемость среди работников трех основных заводов ПО «Маяк». Для них сбор дозиметрической информации производился наиболее полно благодаря практически массовому индивидуальному дозиметрическому контролю.
Начало наблюдения определялось датой найма на ПО «Маяк». Средний возраст найма составил около 23 лет. Средняя продолжительность жизни на дату 31.12.2013 – 59,6 лет. К указанной дате умерло 13 668 мужчин (70,6% списочного состава регистра). Средняя реконструированная эквивалентная доза облучения на стенку мочевого пузыря составила 422,5 мЗв. Использованы коэффициенты эквивалентности для внешнего проникающего излучения и для внутреннего облучения инкорпорированным плутонием. Значения доз определялись кумулятивно на конец жизни или к моменту постановки диагноза РПЖ, в зависимости от того, какое событие означало фактическое прекращение наблюдения. Воздействию ионизирующего излучения с кумулятивными зарегистрированными дозами более некого условного фонового предела в 50 мЗв за всё время наблюдения подвергалось 13875 работников мужского пола. Эта величина меньше доз от естественного радиационного фона за период работы на предприятии. Остальные работники имели производственные дозы, либо не состояли на ИДК и не направлялись на биофизическое обследование на носительство соединений плутония. В среднем в расчете на стенку мочевого пузыря у персонала преобладало внешнее облучение – кумулятивную поглощенную дозу гамма-излучения более 50 мГр получило 13845 человек; кумулятивную дозу внутреннего альфа-облучения более 2,5 мГр получило 455 человек. Таким образом, статистическая возможность связать заболеваемость РПЖ с внутренним облучением представляется весьма призрачной. Ионизирующее воздействие измерено и реконструировано в соответствии с дозиметрической системой MWDS-2013 , , , принятой для производственного объединения «Маяк» в Южно-Уральском институте биофизики ФМБА. Основные характеристики исследованной выборки представлены в сводной Таблице 1.
Таблица 1 - Основные характеристики рассматриваемого регистра
Условия | Характеристики | |
Период наблюдения, годы | 1948 – 2013 | |
Годы найма, годы | 1948 – 1982 | |
Годы рождения, годы | 1886 – 1965 | |
Численность регистра | 19 395 | |
Событий смерти от всех причин | 13 688 | |
Событий смерти от РПЖ | 165 | |
Событий заболевания РПЖ | 298 | |
Возраст самого раннего случая заболевания РПЖ (доза 50 мЗв), лет | 51 | |
Возраст самого раннего случая заболевания РПЖ (доза > 50 мЗв) , лет | 41 | |
Возраст самого позднего случая заболевания РПЖ (доза 50 мЗв) , лет | 87 | |
Возраст самого позднего случая заболевания РПЖ (доза > 50 мЗв) , лет | 91 | |
Техногенные поглощенные дозы на дату окончания наблюдения (доза на стенку мочевого пузыря) | Внеш | 0,04 мГр … 7,31 Гр |
Внутр | 0,0001 мГр … 50,4 мГр | |
Примечание: мужчины
3. Результаты
Хорошо известно, что относительная неопределенность интенсивных (годовых) показателей риска в силу закона больших чисел обратно пропорциональна корню из числа «случаев» в выделенной страте, т.е . Следовательно, наиболее простой способ получения устойчивых оценок в процессе разведки – укрупнение изучаемых страт в ущерб подробной стратификации по эквивалентной дозе. Учитывая весьма длительный характер эпидемиологических наблюдений за персоналом ПО «Маяк», наиболее просто сравнить кумулятивные показатели заболеваемости РПЖ в двух группах сотрудников, имеющих существенные отличия по дозе. Этот приём не позволит выявить характер дозовой зависимости (линейный/ нелинейный/ пороговый/ беспороговый), однако даст возможность статистически устойчивого сравнения по типу «больше ‒ меньше», то есть позволит наблюдать собственно избыточный эффект. Результат такого сравнения по соотношению рисков заболеваемости и смертности показан в Таблице 2.
Таблица 2 - Разведочная оценка связи событий заболевания РПЖ и смерти от РПЖ с дозой ионизирующей радиации
Характер эффекта | Дозы | Дозы | Отношение рисков | p-value по Пирсону | |||
Случаи | Выборка | Случаи | Выборка | ||||
% | n | ||||||
Заболеваемость РПЖ | 249 | 13875 | 49 | 5520 | 95 | 2,02 (1,49‒2,74) | <0,00001 |
Смертность от РПЖ | 133 | 13875 | 32 | 5520 | 95 | 1,65 (1,13‒2,43) | 0,01 |
РПЖ – не первое онкозаболевание | 24 | 13875 | 2 | 5520 | 95 | 4,77 (1,23‒18,48) | 0,02 |
Примечание: все оценки относительного риска для всех трёх таблиц сопряженности статистически значимы на уровне значимости 0,05; оценки доверительных интервалов даны по Zou ‒ Donner
Там же показан довольно интересный эффект связи заболеваемости РПЖ с эквивалентной органной дозой при наблюдении таких случаев, где до наступления изучаемого события у больного регистрировались и другие локализации первичного рака (с кодами 140; 151; 151.0; 151.1; 151.2; 153.0; 153.3; 153.6; 154.0; 161.9; 162.2; 162.3; 162.5; 162.9; 172.4; 172.6; 173.5; 173.6; 175; 188; 189.0; 190; 200.1; 207.1 по МКБ-9, то есть со злокачественными онкологическими заболеваниями желудочно-кишечного тракта, легких, меланомным раком кожи и онкологией мочеполовой системы). Наличие сопутствующего онкологического заболевания увеличивало риск развития РПЖ сильнее, чем прямое воздействие ионизирующей радиации на исследуемый орган.
Таблица 2 исключает сомнения в существовании связи дозы ионизирующей радиации с повышенной заболеваемостью РПЖ, однако она не дает ответа на вопрос о динамике такой связи и о математическом характере дозового тренда. Удивительно, но публикации , , непосредственно посвященные тому же самому регистру, также не дают подобных ответов, несмотря на то, что применявшийся инструмент исследования – алгоритм и код AMFIT – прямо был предназначен для многофакторного анализа трендов показателя интенсивности заболеваемости в динамике. Действительно, если приближенно считать, что все «случаи» в группе сравнения (дозы) являются спонтанными, можно ожидать, что в исследуемой группе (дозы ) число спонтанных РПЖ достигнет примерно 49×(13875/5520) 123. Тогда радиационно-обусловленный избыток будет оцениваться величиной 249 – 123 126. Или с учетом 95%-ной вероятности пуассоновского рассеяния примерно 82 … 158 человек, но отнюдь не 5 человек, как предполагалось ранее .
Главная причина систематических различий полученных результатов и ранее проведенных исследований, на наш взгляд, заключается в неоправданном доверии к безотчетному применению кода AMFIT при анализе редких событий, для которых пуассоновская регрессия, казалось бы, и предназначена. Действительно, судя по публикациям , код AMFIT применялся для набора страт, обусловленных делением на интервалы по 3 факторам, по меньшей мере: доза (17 интервалов), достигнутый возраст (15 интервалов) и календарный год на момент диагностики РПЖ (около 2 интервалов). Общее количество страт – не менее 17×15×2 = 510. Нетрудно понять, что 160 случаев РПЖ невозможно было распределить по этим стратам так, чтобы некоторые из них не оказались пустыми, несущими нулевую ММП-информацию. В таких условиях источником смещений эпидемиологических оценок может являться и малое число случаев в страте, и сам принцип максимального правдоподобия при поиске центральных оценок, и неравномерное распределение «случаев» по стратам. Например, если число случаев в страте меньше 4, то расширенная относительная погрешность оценки показателя риска по одной страте (на уровне 95% вероятности) превышает 100%. В такой ситуации говорить об «измерении эффекта» невозможно. А при стремлении числа случаев к нулю вместе с принципом максимизации правдоподобия добавляется также сопоставимое систематическое смещение оценок.
Не менее важным является правильное описание распределения показателя спонтанной заболеваемости изучаемым раком по достигнутому возрасту. По указанной причине нами выполнены прямые, пусть и грубые, оценки поведения годовой функции спонтанного риска в двух выделенных дозовых группах, аналогичных Таблице 2, в надежде получить оценку в группе сравнения, близкую к фоновой кривой интенсивности заболевания РПЖ. В соответствии с пуассоновским подходом, за эмпирическую оценку интенсивности hazard принималось отношение числа случаев к числу человеко-лет наблюдения согласно общеизвестному эпидемиологическому определению , . Однако, в отличие от , , количество человеко-лет применялось не в качестве традиционно определенной кумулятивно-экспозиционной эпидемиологической категории, а в привязке к наблюдаемой эпидемиологической ступенчатой функции условно-здорового дожития так, как это корректно описано в методе Каплана – Майера и в техническом определении понятия «интенсивность отказов» (ГОСТ 27002–89). При стратификации игнорировались все факторы риска, кроме дозы облучения, достигнутого возраста и наличия у работников в анамнезе 1-х, 2-х и даже 3-х первичных раков наряду с диагностированным РПЖ. В последнем случае такие работники (26 человек) из анализа показателя заболеваемости были исключены. Результаты наблюдений сгруппированы на рисунке 1. Существенной особенностью группировки событий заболеваемости по возрасту являлся такой выбор границ, который гарантирует равномерное распределение «случаев» по возрастным интервалам.
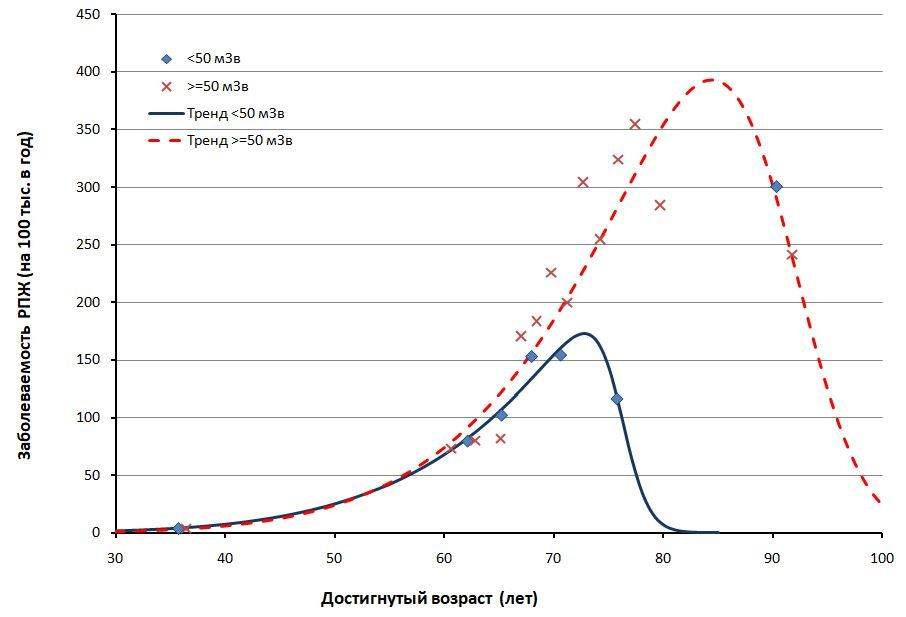
Рисунок 1 - Сопоставление возрастных зависимостей интенсивности заболеваемости РПЖ в разных дозовых группах
Примечание: эмпирические данные получены как непараметрические групповые оценки по возрастным стратам; аппроксимации показателя выполнены на основе концепции «frailty group» Армитажа [20] и Ваупеля [21], [22]
Особо укажем на весьма популярную аппроксимацию , , , для фоновой модели интенсивности заболеваемости hazard (h0):
где ‒ вектор параметров аппроксимации; t достигнутый возраст.
Она имеет определенную мотивацию, которую можно понять, переписав формулу в следующем виде: . Иными словами, это – степенная зависимость функции hazard от t, подправленная слабым логарифмическим трендом в показателе степени. Действительно, в публикации можно найти упоминание о том, что показатели интенсивности онкологической заболеваемости и смертности почти всегда демонстрируют степеннóй рост от достигнутого возраста (тренд Армитажа и Долла). Это позволяет некоторым исследователям даже пренебрегать параметром
в модели , предполагая исключительно рост показателя спонтанной заболеваемости с возрастом. Однако это устаревшие сведения! Современные статистические данные надежно фиксируют не только рост, но и спад годовых показателей риска в типичном диапазоне достигнутых возрастов от 70 до 85+ лет почти для всех солидных раков, что объясняется формированием в течение жизни и истощением уязвимых подгрупп, управляющих динамикой показателя в старших возрастах. Заметим, что на рис. 1 этот эффект (заболеваемость РПЖ) присутствует как для группы сравнения, так и для группы с большими кумулятивными дозами. Следует отметить, что модель (1) с двумя логарифмами для любых параметров
и
близка к так называемому лог-нормальному распределению, благодаря чему кривая hazard всегда скошена влево, то есть имеет длинный спадающий хвост в области больших возрастов. Между тем, на рис. 2 истинная зависимость фонового показателя риска от возраста скошена вправо. Таким образом, выбор модели (1), а вместе с ней и выбор концепции пропорциональных показателей риска при построении дозо-зависимой модели принципиально не способен обеспечить адекватную аппроксимацию эмпирических наблюдений при любой их стратификации.
Недостатком анализа данных, представленных на рис. 1, является невозможность определения дозовой зависимости показателей риска, если стратификация по дозе произведена всего лишь по двум интервалам. Для получения более детальных сведений нами был всё-таки использован алгоритм AMFIT, но с учётом тех поправок и ограничений, которые диктуются его истинной природой метода минимальной девиации и невозможностью применения произвольно-частой стратификации пространства факторов. Именно эти два качества никак не документированы, но реально присутствуют в опубликованном популярном алгоритме .
Очевидно, при ограничении на заселенность предельная стратификация регистра ПО «Маяк» по РПЖ допускает примерно
страт. При одновременном учёте в качестве факторов риска дозы гамма-облучения и возраста, можно рассчитывать на разбиение 7 × 7. Оказывается при этом, даже контролируя равномерность маржинальных распределений изучаемых событий как по дозе, так и по возрасту, удается получить лишь далёкое от равномерного фактическое заселение страт с частотами от 1 до 12. Среди них 9 страт пришлось вообще удалить из анализа и ещё 13 страт имели пограничные частоты
.
Поэтому практически пришлось вынужденно работать с меньшим уровнем стратификации, например 5 × 5 (Таблица 3), что позволило различить всего 5 градаций по дозе. Для наблюдений характерна ярко выраженная зависимость от возраста, и очень слабая зависимость избыточного риска от дозы. Результат сравнительной минимизации девиации AMFIT для ряда моделей, включая традиционные, линейные по дозе – приведен в Таблице 4. Итого рассмотрено 2 группы основных конкурирующих моделей (гипотез): традиционные почти степенные (2) и модели на базе концепции «frailty group» (3):
Таблица 3 - Двухфакторное распределение наблюдений по стратам
Номер страты | Случаи | Человеко-годы под риском | Средний возраст найма, лет | Средний возраст в страте, лет | Доза гамма, мЗв | Грубый показатель (на 100000) в год |
0 | 16 | 210678,0 | 21,6 | 39,5 | 20,4 | 7,6 |
1 | 13 | 11895,3 | 22,6 | 65,3 | 21,2 | 109,3 |
2 | 12 | 7093,9 | 23,2 | 69,8 | 23,0 | 169,2 |
3 | 8 | 4910,3 | 25,6 | 74,0 | 20,8 | 162,9 |
4 | 8 | 4184,6 | 27,2 | 79,1 | 22,1 | 191,2 |
5 | 13 | 138378,0 | 21,4 | 40,3 | 111,3 | 9,4 |
6 | 14 | 8537,6 | 22,3 | 65,3 | 113,7 | 164,0 |
7 | 11 | 5066,7 | 23,3 | 69,8 | 117,0 | 217,1 |
8 | 10 | 3604,5 | 23,9 | 74,0 | 117,7 | 277,4 |
9 | 6 | 3340,9 | 26,0 | 79,2 | 118,2 | 179,6 |
10 | 8 | 105680,0 | 22,6 | 40,9 | 260,7 | 7,6 |
11 | 12 | 7820,2 | 23,0 | 65,5 | 259,5 | 153,4 |
12 | 15 | 5214,8 | 23,4 | 69,9 | 260,4 | 287,6 |
13 | 11 | 3965,8 | 23,2 | 74,0 | 264,0 | 277,4 |
14 | 8 | 3865,9 | 25,1 | 79,4 | 270,5 | 206,9 |
15 | 6 | 101448,0 | 23,8 | 41,4 | 569,2 | 5,9 |
16 | 8 | 8138,1 | 24,1 | 65,5 | 562,1 | 98,3 |
17 | 10 | 5599,9 | 24,3 | 69,9 | 563,4 | 178,6 |
18 | 11 | 4451,9 | 24,1 | 74,1 | 564,1 | 247,1 |
19 | 17 | 4387,7 | 24,5 | 79,4 | 564,5 | 387,4 |
20 | 11 | 104701,0 | 24,2 | 41,7 | 1631,0 | 10,5 |
21 | 7 | 8316,5 | 24,9 | 65,5 | 1697,0 | 84,2 |
22 | 7 | 5574,5 | 24,9 | 69,8 | 1739,0 | 125,6 |
23 | 14 | 4234,9 | 25,6 | 74,0 | 1722,0 | 330,6 |
24 | 16 | 4926,0 | 25,5 | 79,8 | 1584,0 | 324,8 |
Примечание: заболеваемость РПЖ
Таблица 4 - Результаты аппроксимации данных по различным моделям в режиме работы AMFIT в качестве метода минимальной девиации
Модель | Ωmin AMFIT | Кол-во парам. | ЧСС |
H00 | 19,93 | 3 | 22 |
H10 | 19,93 | 4 | 21 |
H20 | 19,93 | 5 | 20 |
norm(t) | — | — | — |
H0 | 238,3 | 1 | 24 |
H1 | 13,77 | 4 | 21 |
H2 | 14,07 | 4 | 21 |
H3 | 15,27 | 3 | 22 |
Примечание: в моделях H0...3 параметры формы β1, β2, β3 функции norm(t) фиксированы; в моделях H1...3 фиксирован также кумулятивный параметр β0; ЧСС – число степеней свободы
Судя по Таблице 4, остаточная девиация для типичных традиционных моделей не была минимальной при любом количестве параметров от 3 до 5, что свидетельствует о неразличимости трендов по дозе как с учетом зависящей от возраста радиочувствительности, так и в предположении её постоянства. В то же время модели на базе концепции «frailty group» с модулирующими поправками по дозе и возрасту или только по дозе обеспечили статистически значимый минимум. Иными словами, удалось найти решение лучшее, чем максимально-правдоподобное по алгоритму AMFIT, не покидая рамок этой методологии. Здесь уместно напомнить утверждение известной теоремы статистического анализа (Харольд Крамер, ): «Не существует другого метода обработки результатов эксперимента, который дал бы лучшее приближение к истине, чем метод максимального правдоподобия». Поскольку более оптимальная оценка всё же найдена, в контексте сравнения теоремы с Таблицей 4 следует признать, что метод AMFIT всё-таки не вполне можно характеризовать как метод максимального правдоподобия, но тем не менее, он позволяет найти заметно лучшую аппроксимацию функций hazard. Причина в том, что ряд его ранее недокументированных методических недостатков частично удалось скорректировать за счет:
а) более правильного выбора фоновой модели риска;
б) более правильной стратификации данных;
в) отказа от моделей пропорционального риска.
Среди совокупности рассмотренных конкурирующих моделей наилучшими по минимуму достигнутой девиации являются
, с предпочтением в пользу модели
, поскольку она немного выигрывает при сравнении с
по информационному критерию Акаике. Примеры расчёта дозо-возрастных трендов по
приведены на рис. 2, который неплохо согласуется с выполненными ранее разведочными непараметрическими оценками.
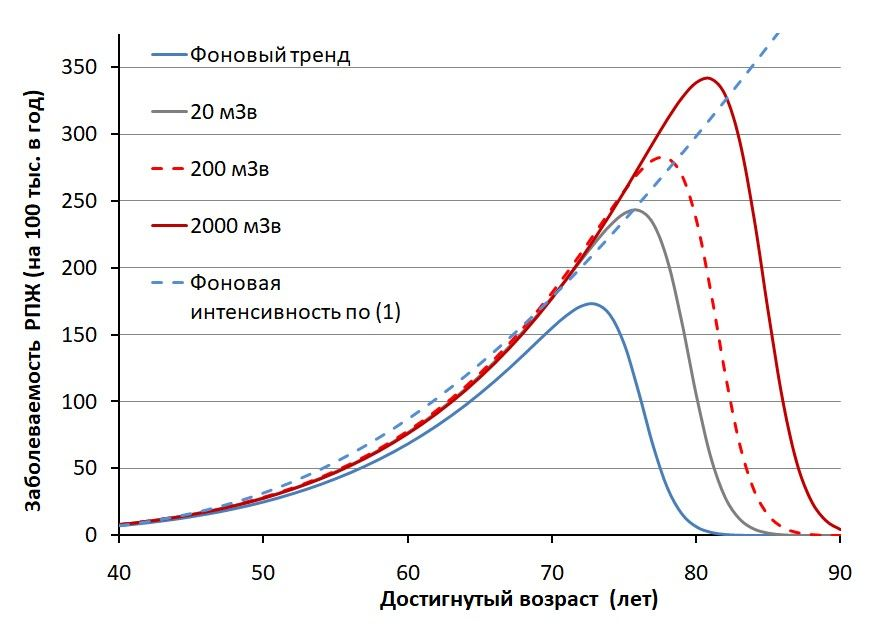
Рисунок 2 - Параметрические оценки дозо-возрастного тренда показателя заболеваемости РПЖ в когорте ПО «Маяк» в соответствии с гипотезой H3
4. Обсуждение
Оценка медицинских последствий профессионального облучения среди персонала ПО «Маяк» позволяет с уверенностью говорить о наличии дозо-зависимого избыточного радиогенного риска РПЖ. В предшествующих исследованиях этот тренд не удавалось уверенно зафиксировать статистико-эпидемиологическими методами наблюдения только благодаря неочевидным ошибкам применения известных статистических алгоритмов, формалистическому подходу к описанию спонтанных рисков и очень специфическим особенностям процесса развития этого вида рака, возможно связанным с его гормонально-зависимой природой. Ранее выполненные исследования не оправдали себя практикой селекции гипотез за счёт применения теста отношения максимальных правдоподобий без проверки качества аппроксимации всей модели. Как оказалось, ошибочными также были ранее предпринятые попытки описать радиогенную составляющую интенсивности возникновения РПЖ с помощью единственного параметра избыточного относительного риска на единицу дозы (ИОР/Зв или ИОР/Гр). Если он и может применяться в отношении РПЖ, то только в том случае, если под термином «риск» понимается кумулятивная величина за определенный продолжительный промежуток времени, то есть вероятность события. Например, в рамках гипотезы, соответствующей рис. 2, получаются оценки, показанные графически на рис. 3. Они указывают на существенно нелинейный характер отклика на радиационное воздействие для изучаемой локализации, но в то же время численно соответствуют результатам в когорте LSS , , оцененным по линейной модели. Благодаря нелинейному эффекту (рис. 2), число радиогенных случаев РПЖ в нашей работе оказалось выше оценок более, чем на порядок.
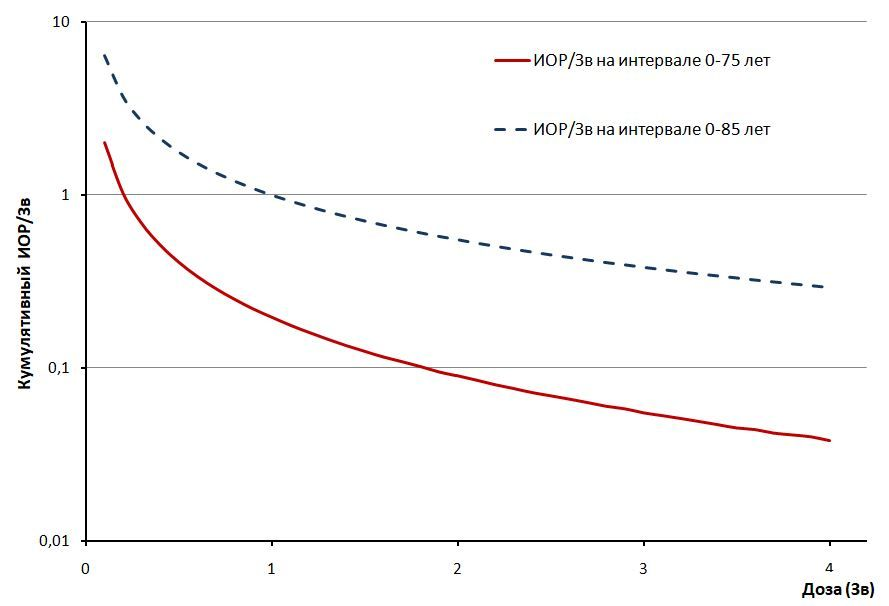
Рисунок 3 - Переменный характер дозового тренда коэффициента избыточного относительного кумулятивного риска на 1 Зв при развитии РПЖ в диапазоне умеренных и больших доз
Примечание: два различных возрастных интервала
Таблица 5 - Оценка отношения кумулятивных рисков (ОР) при попарном сравнении дозовых страт
Кумулятивная доза, Гр | Чел.-годы под риском | Случаи РПЖ | ОР (90% ДИ), к нулевой страте | p, (ОР<1) |
0 | 76726 | 4 | 1 | 0,5 |
(0‒ 0,01] | 29740 | 5 | 3,13 (1,12 ‒ 9,02) | 0,034 |
(0,01‒ 0,1] | 101164 | 17 | 2,87 (1,30 ‒ 7,30) | 0,013 |
(0,1‒ 0,5] | 119365 | 67 | 9,31 (4,60 ‒ 22,5) | <10-10 |
(0,5‒ 1] | 42345 | 30 | 11,90 (5,65 ‒ 29,4) | ≈10-10 |
(1‒ 2] | 35201 | 25 | 11,98 (5,62 ‒ 29,8) | <10-9 |
2+ | 12392 | 12 | 16,79 (7,25 ‒ 43,8) | <10-8 |
Математическая обработка в Таблице 5 выполнена байесовским методом при условии допустимости применения равномерного приора к пуассоновскому закону распределения счётных событий. С использованием алгоритма AMFIT для дозовых страт на рис. 4 по тесту отношения правдоподобий произведено сравнение нелинейного тренда с двухпараметрическим линейным. В результате гипотезу линейности пришлось полностью отвергнуть Для неё минимальное значение насыщенной пуассоновской девиации достигало значения
, которое существенно превосходило число степеней свободы
. Это обстоятельство совершенно не позволяло считать наблюдаемые отклонения показателей риска от линейного тренда случайными. Если бы в работах , , , авторы обращали внимание на соотношение
и
для подтверждения качества аппроксимаций вместо теста отношения правдоподобий, они тоже отвергли бы предположения о линейности по дозе.
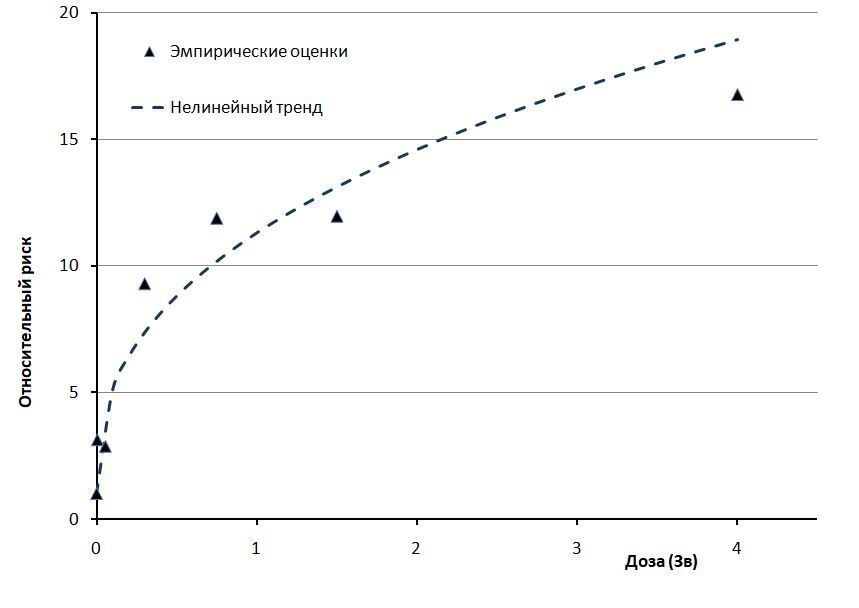
Рисунок 4 - Фактически наблюдавшийся в работе нелинейный дозовый тренд отношения кумулятивных рисков заболевания РПЖ, ошибочно принятый за линейный
Примечание: по ист. [8]
Полученные результаты определенно свидетельствует о неприменимости моделей пропорционального риска или линейных моделей, по меньшей мере, к анализу заболеваемости РПЖ. Следовательно, в отношении РПЖ в широком диапазоне возрастов или доз нельзя в качестве меры тренда использовать популярные постоянные характеристики ИОР/Зв. Динамика формирования показателей риска заболеваемости должна иметь какое-то другое объяснение. Очевидно, показатель риска hazard не может безынерционно реагировать на ионизирующее излучение.
5. Заключение
Установлено, что в когорте персонала ПО «Маяк» присутствует статистически различимая связь между повышенными показателями риска заболеваемости раком предстательной железы и воздействием ионизирующей радиации на рабочих местах. Однако её невозможно интерпретировать в рамках популярной линейно-беспороговой теории в силу нарушения линейного характера отклика показателей риска на кумулятивную дозу. По показателю Нельсона-Аалена на возрастном интервале от 25 до 75 лет для кумулятивной дозы на стенку мочевого пузыря 1 Зв коэффициент дозового тренда избыточного кумулятивного риска составил ИОР/Зв = 19,7 %·Зв‒1; а для 0,25 Зв — ИОР/Зв = 41,1 %·Зв‒1. Эти результаты, являясь более обоснованными по сравнению с публикациями , , , , всё же не дают никакого рационального объяснения наблюдаемой нелинейной природе зависимости показателей риска РПЖ в когорте от дозы. Ясно, что поиск объяснения результата уже не должен производиться на основе эвристических моделей (2, 3), статических по существу. Для прогнозирования групповых радиационных эффектов следует в будущем использовать динамические модели формирования показателей риска, связывая их с историей облучения на рабочих местах. Эта задача, однако, выходит как за рамки известных непараметрических методов, так и за рамки возможностей алгоритма AMFIT. Для корректной оценки избыточной (радиогенной) заболеваемости в условиях хронического облучения требуется создание нового инструмента её статистической оценки.
Превышение годовых показателей интенсивности заболевания РПЖ над спонтанным уровнем уверенно регистрируется только в диапазоне возрастов 70+ лет. Избыточная часть общей заболеваемости запаздывает по отношению к спонтанной, что приводит к неприемлемости прогнозирования индивидуальных радиационных эффектов с помощью моделей пропорционального риска, связывающих дескриптивную интенсивность заболеваемости («мгновенный» показатель) и кумулятивную дозу. По крайней мере, в случае анализа заболеваемости РПЖ, кумулятивные дозы могут применяться только для предсказания кумулятивных групповых эффектов. По состоянию на конец 2013 года можно утверждать, что из 298 заболеваний РПЖ, наблюдавшихся на предприятии среди 19 395 мужчин, от 82 до 158 случаев были радиационно-обусловленными (при среднем уровне кумулятивных эквивалентных доз около 0,42 Зв). Однако в целом по когорте предприятия без учета радиационного воздействия кумулятивные показатели заболеваемости были ниже или были сопоставимы со средними показателями в Российской Федерации.
Радиационный риск развития рака предстательной железы, являющегося гормонально-зависимым заболеванием, оказался также существенно зависящим от других предшествующих заболеваний, прежде всего, онкологических. Наблюдается мультипликативное взаимодействие радиационных и онкологических факторов риска.
В ходе исследования выявлены недокументированные ограничения возможностей статистического пакета Epicure (модули AMFIT и DATAB), являющегося международно-признанным стандартом «de facto» при проведении радиационно-эпидемиологического анализа.
